서론
PFAPA(periodic fever, aphthous stomatitis, pharyngitis, and adenitis) 증후군은 소아기 재발성 발열(recurrent fever)의 가장 흔한 원인으로, 주기적 발열(periodic fever)과 아프타 구내염(aphthous stomatitis), 인두염(pharyngitis), 경부 림프절염(cervical lymphadenitis)을 특징으로 하는 자가염증 질병(autoinflammatory disease, AID)이다[1-3]. 1987년 Marshall et al.[2]이 원인 미상의 주기적 발열 환자 12명을 처음으로 보고하였고, 그 후 PFAPA 증후군이라 명명하였다[3]. PFAPA는 자기한정적(self-limiting) 질병으로, 환자의 대부분은 10세 이후 더 이상 주기적 발열을 나타내지 않는다[2,4].
Ohnishi et al.[5]은 일본에서 가와사키병(Kawasaki disease, KD)이나 전신형 소아기특발성관절염(systemic juvenile idiopathic arthritis, SJIA)과 같은 AID 발생률이 높은 것처럼, 일본의 실제 PFAPA 발생률은 보고된 것보다 휠씬 높을 수 있다고 주장하였다. 국내 PFAPA 연구는 지금까지 대여섯 편의 논문만 발표되었을 정도로 매우 제한적이지만, 일본과 유사하게 우리나라의 실제 PFAPA 발생률도 과소평가되었을 수 있다[6-11]. 부족한 연구와 상반되게, 일부 보호자들은 부정확한 의학정보로 인해 자녀의 PFAPA 이환 가능성에 대해 지나치게 염려하기도 한다[12,13].
이러한 의학적, 사회적 이유를 고려하면, PFAPA를 주로 진료하고 연구하는 전문가가 아닌 일차 진료의들도 PFAPA에 대한 기본적 이해가 필요할 것이다[1]. 본 연구에서 저자들은 PFAPA의 역학, 임상양상, 진단, 감별진단 및 치료에 대해 기술하고, 최근 소아기 재발성 발열의 원인으로 주목받고 있는 새로운 자가염증 질환군을 소개하려고 한다.
본론
여러 인종과 국가에서 PFAPA의 발생이 보고되었다. 5세 이하 소아의 PFAPA 발생률은 노르웨이 연구[14]에서 23/100,000명이었고 핀란드 연구[15]에서는 20/100,000명이었다. 성비는 남아의 비율(~1.8:1)이 다소 높았다. 호발 연령은 1-4세이지만, 환자의 10%-20%는 5세 이후 발생하고 일부 환자는 성인이 된 후 발생한다[4,15].
구체적인 병리기전은 밝혀지지 않았지만, 유전적 감수성(genetic susceptibility)은 PFAPA 발생의 필수적인 요소이다[16-18]. 하지만 단일유전자(monogenic) 변이가 확인된 유전성 재발성 발열(hereditary recurrent fever, HRF)과 달리, PFAPA는 복합유전자(polygenic) 이상에 의해 발생된다[19,20]. 일부 PFAPA 환자에서 명확한 가족력이 증명되는데, 이때는 상염색체 우성(autosomal-dominant) 유전 방식을 보인다[17]. 주요한 4대 HRF, 즉 i) 가족성 지중해 발열(familial Mediterranean fever, FMF; MEFV), ii) 종양괴사인자 수용체관련 주기증후군(tumor necrosis factor receptor-associated periodic syndrome, TRAPS; TNFRSF1A), iii) 크리오피린관련 주기증후군(cryopyrin-associated periodic syndrome, CAPS; NLRP3) 및 iv) 메발론산 인산화효소 결핍증(mevalonate kinase deficiency, MKD; MVK; 과거의 hyperimmunoglobulin D syndrome, HIDS)의 유전자 변이가 PFAPA 환자에서 관찰될 수 있다[17,19]. 특히 FMF유전자(MEFV) 관련 보고가 많았는데, 실제로 터키와 이스라엘 등 지중해 지역의 PFAPA 환자 중 ~20%는 FMF도 동시에 진단된다[20].
반복적 아프타 구내염(recurrent aphthous stomatitis) 및 베체트병(Behçet disease, BD)과 임상 표현형(clinical phenotype)과 유전자형(genotype)이 유사하여, PFAPA를 베체트 범주 질환군(Behçet spectrum disorders, BSD)에 포함시키기도 한다[21,22]. 임상양상의 심한 정도는 반복적 아프타 구내염 < PFAPA < BD의 순이다[22].
주기적 발열은 PFAPA의 가장 중요한 특징이다. 전형적 PFAPA 환자는 28일(범위: 14-42일) 주기로, ~41.0°C의 발열을 4일(범위: 2-7일) 동안 나타낸다[12,13]. 주기성 없는 불규칙한 발열이나 7일 이상 길어지는 발열을 보이는 환자에서는 PFAPA 이외의 다른 원인을 고려해야 한다[10,11]. ‘발열기(fever episodes)’의 혈액검사에서 백혈구증가증(~18,000 /μL)과 적혈구 침강속도(erythrocyte sedimentation rate, ESR), C-반응단백(C-reactive protein, CRP; 범위: 12-18 mg/dL), 아밀로이드 A(amyloid A) 등 급성기 반응물질(acute phase reactant, APR)의 증가가 관찰된다[23,24]. 프로칼시토닌(procalcitonin)은 일반적으로 증가하지 않는다[25]. 다음 주기적 발열이 시작되기 전까지 환자는 특별한 증상을 보이지 않고 건강하다. 따라서 성장과 발달에 문제가 없다.
아프타 구내염은 입술 안쪽, 볼점막(buccal mucosa) 및 후인두부에 나타난다. 특징적 병변이지만, PFAPA의 핵심증상 중 가장 낮은 빈도로 관찰된다[14,15]. 인두염은 주기적 발열 다음으로 흔한 핵심증상으로 삼출물이 동반되기도 한다. 경부 림프절염은 환자의 ~3/4에서 관찰된다[26]. Table 1에는 PFAPA의 다양한 임상양상을 요약하였다.
| Unite States (n = 94) [26] (%) | Europe (n = 301) [27] (%) | Japan (n = 100) [5] (%) | Korea (n = 17) [10] (%) | |
|---|---|---|---|---|
| Essential features | ||||
| Periodic fever | 100 | 100 | 100 | 100 |
| Aphthous stomatitis | 67 | 57 | 49 | 18 |
| Pharyngitis | 65 | 90 | 89 | 100 |
| Adenitis, cervical | 77 | 78 | 50 | 88 |
| Additional features | ||||
| Abdominal pain ± diarrhea | 45 | 59 | 31 | 30 |
| Headache | 65 | 29 | 10 | 23 |
| Rash | 15 | 13 | - | 6 |
| Arthralgia or arthritis | - | 39 | - | 6 |
| Lips or tongue changes | - | - | - | 12 |
| Conjunctivitis | - | 5 | - | - |
| Chest pain or cough | 20 | - | - | - |
Table 2에는 주요한 PFAPA 진단기준을 나타냈다. 1999년 발표된 Thomas 기준[26]은, i) 5세 미만 소아에서 주기적 발열, ii) 상기도 감염 등 다른 발열의 원인 없이 PFAPA 3대 증상(아프타 구내염, 인두염 및 림프절염) 중 1개 이상 관찰, iii) 주기성 중성구감소증(cyclic neutropenia)의 배제, iv) 발열기 사이에는 무증상 및 v) 정상적인 성장과 발달, 총 5가지 항목을 만족하는 환자를 PFAPA로 진단한다. Thomas 기준을 수정된 Marshall 기준(modified Marshall criteria)이라 부르기도 한다. 2016년 Lantto et al.[15]은 주기적 발열의 횟수 5회 이상, 요로감염 및 HRF의 배제 등을 추가하여 Thomas 기준을 보완하였다. 또한, PFAPA 3대 증상이 없더라도 편도제거술(tonsillectomy) 후 주기적 발열이 완전히 호전되면 PFAPA로 진단할 것을 제안하였다.
| Thomas criteria (1999) [26] | PRINTO criteria (2019) [30] |
|---|---|
| All of 5 criteria | At least 7 of 8 criteria |
| 1. Periodic Fever in children < 5 years of age with history of ≥ 5 fever episodes1) | 1. Presence of periodicity |
| 2. Presence of fever for 3–6 days | |
| 2. At least 1 of 3 essential symptoms in absence of URIs or UTIs1) | |
| i) Aphthous stomatitis | |
| ii) Pharyngitis | 3. Presence of pharyngitis |
| iii) Adenitis, cervical | 4. Presence of cervical (lymph-)adenitis |
| 3. Exclusion of cyclic neutropenia and monogenic HRF1) | 5. Absence of diarrhea |
| 4. Asymptomatic interval between fever episodes | 6. Absence of arthritis |
| 5. Normal growth and development | 7. Absence of skin rash |
| Therapeutic diagnosis through tonsillectomy1,2) | 8. Absence of chest pain |
The criteria were supplemented by Lantto et al. (2016) [15].
2019년 유럽 소아 류마티스학회(Paediatric Rheumatology European Society, PRES) 산하의 소아 류마티스 국제 임상연구 기구(Paediatric Rheumatology International Trials Organisation, PRINTO)에서 281명 전문가들의 합의된 분류기준(consensus classification criteria)를 발표하였다[30]. 이 기준은 PFAPA 환자의 존재(presence) 항목 4가지와 부재(absence) 항목 4가지, 총 8가지 항목으로 구성된다. PRINTO 기준은 진단의 민감도(97%)와 특이도(93%)가 우수하다. 하지만, 아직까지 대부분 연구에서는 Thomas 기준을 많이 사용한다[31,32]. 모든 PFAPA 환자가 Thomas 기준의 5가지 항목을 완전히 만족하지는 않는다[5,15]. 예를 들어, 5세 이후 발생하거나 성장지연이 동반되어 4개 항목만 충족하는 환자는 ‘불완전(incomplete) PFAPA’로 정의할 수 있다[5].
PFAPA를 조기에 인식하여 적절한 치료하는 것은 불필요한 검사를 줄이고 예후를 향상시키는 가장 좋은 방법이다[11,19]. 지금까지 알려진 것보다 휠씬 많은 PFAPA 환자들이 재발성 발열 소아 중에 존재할 수 있다[6-9]. 하지만 이와는 상반되게, 반복적인 감염으로 인한 빈번한 발열을 PFAPA로 과장되게 진단할 수도 있다[10,11]. 즉, 실제 임상에서는 PFAPA의 과소 진단(under-diagnosis)과 과잉 진단(over-diagnosis) 가능성을 동시에 염두해야 한다.
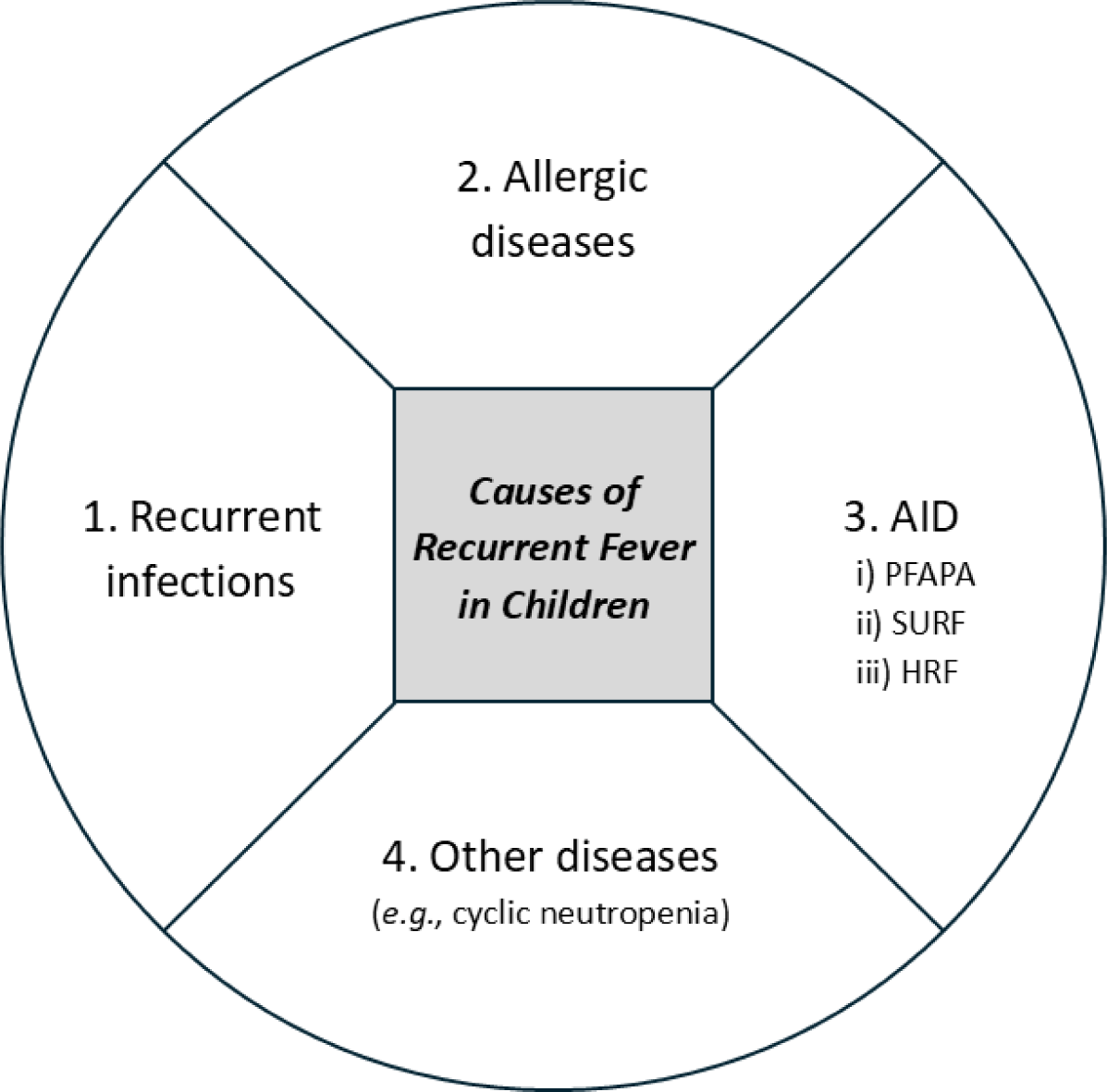
PFAPA는 임상증상을 토대로 진단하는 질병이므로, 재발성 발열을 특징으로 하는 다른 소아기 질병을 배제하는 것은 진단의 전제조건이다(Fig. 1). 감별진단에서 흔하게 마주치는 질환은 반복적 감염(recurrent infections)이다[33,34]. PFAPA가 없는 어린 소아들은 연간 6-8회 바이러스 감염질환을 경험한다[33]. 알레르기 질환(allergic disease)이 동반된 소아들은 좀더 빈번하고 심한 증상을 나타낸다[34]. 즉, 반복적 감염이나 알레르기 질환에 의한 재발성 발열이 PFAPA로 오인될 수 있다[35]. 발열기에 PFAPA의 가족 구성원들은 대개 무증상이지만, 감염질환의 가족 구성원들은 환자와 유사한 증상을 보이는 경우가 흔하다[33]. 또한, APR은 발열기 PFAPA에서 증가하지만 일반적인 바이러스 감염질환에서는 증가하지 않는다[36]. 하지만, 홍역 등 일부 바이러스 감염과 세균 감염에서는 APR이 증가하기 때문에, 상황에 따라 발열의 원인을 구분하기 위한 미생물학적 평가가 필요하다[36,37].
PFAPA와 실제적으로 감별이 필요한 질환은 주요한 4대 HRF (FMF, TRAPS, CAPS 및 MKD)이며, 이는 Thomas 기준에 반영되었다[15,26]. HRF은 PFAPA보다 발생빈도는 낮지만(~1/100,000명), 전반적으로 심한 임상경과를 보이며 10세 이후에도 증상이 지속된다[10,12]. HRF은 재발성 발열이 특징이지만, MKD 외에는 주기성 없는 불규칙한 발열을 나타낸다. 또한 PFAPA와 비해, HRF에는 복통, 두통, 피부발진, 관절통, 흉통 등 추가 증상이 흔하게 동반된다[11,19]. 따라서, 10세 이후 심한 증상, 주기성 없는 불규칙한 발열, 혹은 우세한 추가 증상을 보이는 환자에서는 HRF을 배제하기 위한 유전자 검사를 고려해야 한다.
PFAPA를 진단하기 위해서는 HRF뿐만 아니라 ‘주기성 중성구감소증(cyclic neutropenia)’의 배제가 필수이다[15,26]. 주기성 중성구감소증은 매우 드문(< 0.1/100,000명) 선천 혈액질환(congenital hematologic disorder)으로, 21일(범위: 14-35일) 주기의 발열과 구내염, 인두염, 복통 등 PFAPA의 임상양상을 나타낸다[38-40]. 발열기에 절대 중성구 수(absolute neutrophil count, ANC)의 감소가 특징이므로, 발열과 함께 중성구감소증(ANC, 0-200 /μL)이 반복되는 환자는 혈액질환 전문가의 자문이 필요하다[31,32]. Table 3에는 소아기 재발성 발열의 원인이 되는 주요한 ‘자가염증 질병들(AID)’과 주기성 중성구감소증의 특징을 비교하였다.
PFAPA: periodic fever, aphthous stomatitis, pharyngitis, and adenitis; SURF: syndrome of undifferentiated recurrent fever; HRF: hereditary recurrent fever; FMF: familial Mediterranean fever; TRAPS: tumor necrosis factor receptor-associated periodic syndrome; CAPS: cryopyrin-associated periodic syndrome; MKD: mevalonate kinase deficiency; HIDS: hyperimmunoglobulin D syndrome; ER: endoplasmic reticulum; AD: autosomal dominant; AR: autosomal recessive; NOMID: neonatal onset multisystem inflammatory disease.
Table 4에는 현재 PFAPA 환자에 적용되는 치료방법을 요약하였다[12,40]. 단일유전자 변이의 HRF와 달리 PFAPA는 양성(benign) 경과의 질병이므로, 치료의 이점과 부작용 그리고 보호자의 선호도를 고려하여 적절한 치료방법을 선택한다.
연구에 따라 차이를 보이지만, PFAPA 환자의 20%-50%는 특별한 치료없이 호전된다[23]. PFAPA 환자는 성장하면서 증상이 점차 경해지고, 발열기를 건너뛰기도 한다. 해열제나 비스테로이드 항염증제(nonsteroidal anti-inflammatory drugs, NSAIDs)는 효과가 입증되지는 않았으나 증상 완화를 위해 보조적으로 사용할 수 있다[27,29]. 많은 보호자들은 대증요법보다는 좀 더 적극적인 치료를 선호한다[13,14].
스테로이드는 PFAPA 치료에 확실한 효과가 입증되었다[41-43]. 발열기가 시작될 때, 경구 스테로이드(prednisone 1-2 mg/kg/dose)를 복용하면 대부분의 PFAPA 환자들은 수 시간 이내 해열된다[42]. 12-24시간 이내 발열이 다시 발생하는 환자(~25%)는 동일 용량의 스테로이드를 한 번 더 복용할 수 있다[43]. 스테로이드 치료가 주기적 발열을 예방하지는 못한다. 일부 환자에서 스테로이드 치료 후 다음 발열기가 빨라진다[44]. 스테로이드 치료를 받은 PFAPA 환자에서 불안감과 소화불량과 같은 일시적인 부작용이 나타날 수 있다[44,45]. 환자가 성장하면서 주기적 발열이 완화되면 스테로이드 치료를 중단한다.
시메티딘은 PFAPA 발열기를 늦추고 심한 정도를 완화시키며 일부 환자에서 완치 효과를 보여, 치료 및 예방 목적으로 사용한다[4,5]. 예방 목적으로는 시메티딘(10-30 mg/kg/day, 최대 800 mg/day)을 6-12개월 동안 사용한다[5]. FMF 예방에 사용되는 콜키신(4-6세 0.5-1.2 mg/day, 6세 이상 1.0-1.8 mg/day)도 시메티딘과 유사하게 PFAPA 예방 효과를 보인다[46].
스테로이드, 시메티딘 등 약물치료에 반응이 없거나 일상 생활에 지장을 초래하는 심한 임상양상을 보이는 PFAPA 환자에서 편도제거술을 고려한다[47]. Licameli et al.[31]은 편도제거술을 받은 PFAPA 환자의 97%(99/102)는 주기적 발열이 완치되었다고 보고하였다. 편도제거술을 받은 환자의 절반 정도는 아프타 구내염, 인두염 및 림프절염 증상도 호전된다[15]. 드물지만, 수술 후 편도 조직이 재생되어(regrow) 주기적 발열이 재발되기도 한다[48]. 편도제거술은 성인 PFAPA 환자에서도 효과가 있지만, 완치 비율은 소아 환자보다 낮다[49].
2020년 Broderick et al.[34]은 재발성 발열 환자(n = 65) 중에서 PFAPA 진단기준과 주요한 4대 HRF 진단기준, 모두를 만족하지 못하는 제3의 ‘자가염증(autoinflammatory)’ 질환군(22%, 14/65)을 확인하여 ‘미분화 재발성 발열 증후군(SURF)’이라 명명하였다.
SURF는 PFAPA와 동일하게 재발성 발열과 전신염증을 특징으로 한다[53-55]. 하지만, 발열은 주기성 없이 불규칙하며 발열 횟수(3회/6개월)도 PFAPA보다 적다[53]. SURF 환자에서 PFAPA와 유사한 구내 궤양(~30%), 인두염(~20%) 및 림프절염(~38%)이 관찰된다[33]. 추가 증상으로 복통이 흔하고 관절통, 피로감(fatigue) 및 안과적 문제도 동반된다[35]. PFAPA와 마찬가지로, 발열기 사이에는 무증상이며 성장과 발달에 문제가 없다. SURF의 병인에는 감염이나 알레르기 등 복잡한 다인자(multifactorial) 요소가 관여한다고 알려져 있다[54]. 실제로 SURF 환자의 상당수는 과거력에 알레르기 병력(~40%)이 있고 가족력에 재발성 발열 병력의 가족 구성원(~30%)이 존재한다[34]. 아직까지 SURF가 PFAPA의 아형인지, 아니면 PFAPA와 무관한 별개의 질병인지 밝혀지지 않았다[55].
SURF 치료에 PFAPA의 치료방법이 적용된다[35]. 스테로이드 치료와 편도제거술로 SURF의 재발성 발열이 호전되지만 치료 효과는 PFAPA에 비해 좋지 않다[53]. 반면 PFAPA 치료에 효과가 미비한 NSAIDs와 몬테루카스트(montelukast)는 SURF 치료에 좋은 결과를 보인다[33,34]. 지금까지 국내에 SURF 관련 보고는 없었으나, 재발성 발열 환자 중에서 적지 않은 SURF 환자가 존재할 것이라 추정된다. Table 5에는 재발성 발열 소아에서 SURF를 임상적으로 의심해야 하는 상황을 나타냈다.
Broderick et al.[34] reported that arthralgia and fatigue were less common than gastrointestinal symptoms.
결론
PFAPA는 소아에서 재발성 발열을 일으키는 가장 흔한 ‘자가염증 질병(AID)’이다. PFAPA 진단을 위해, Thomas 기준이나 PRINTO 기준에 포함되는 특징적 임상양상을 확인하고 소아기 재발성 발열의 다른 원인들, 즉 반복적 감염, 알레르기 질환, HRF와 SURF를 포함한 다른 AID 및 주기성 중성구감소증 등을 배제해야 한다. 지금까지 보고된 것보다 휠씬 많은 PFAPA 환자들이 재발성 발열 소아 중에 존재할 수 있다. 반면에 단순히 발열이 반복된다는 이유로, 일부 환자들은 성급하게 PFAPA로 진단되거나 PFAPA에 대한 복잡한 검사를 받을 수 있다. 따라서 실제 임상에서 PFAPA가 의심되는 환자를 적절하게 구분하기 위해서는 일차 진료의도 PFAPA에 대한 기본적 이해가 필요하다.
